W latach 2018-2022 Ministerstwo Zdrowia zrefundowało nowe terapie lekowe w chorobach rzadkich nieonkologicznych: choroba Fabry’ego, Duchenne’a, Cushinga i Wilsona, rdzeniowy zanik mięśni, akromegalia, hemofilia A i B u dzieci, mukowiscydoza, tętnicze nadciśnienie płucne, pierwotna hiperoksaluria typu 1, nocna napadowa hemoglobinuria, ostra porfiria wątrobowa, fenyloketonuria, wrodzony obrzęk naczynioruchowy, cystynoza nefropatyczna, zwyrodnienie wielotorbielowate nerek, zespół miasteniczny Lamberta-Eatona, anemia aplastyczna i pierwotna małopłytkowość immunologiczna. Także chorzy na nowotwory krwi i rzadkie guzy lite otrzymali dostęp refundacyjny do nowych leków w terapii przewlekłej białaczki limfocytowej i szpikowej, ostrej białaczki limfoblastycznej i szpikowej, szpiczaka plazmocytowego, chłoniaków złośliwych, mielofibrozy, mastocytozy oraz raków kolczystokomórkowego, wątrobowokomórkowego, tarczycy i raka z komórek Merkla.
Według danych Ministerstwa Zdrowia w 2021 r. na zrefundowanych 68 nowych cząsteczko-wskazań, aż 29 dotyczyło chorób rzadkich.
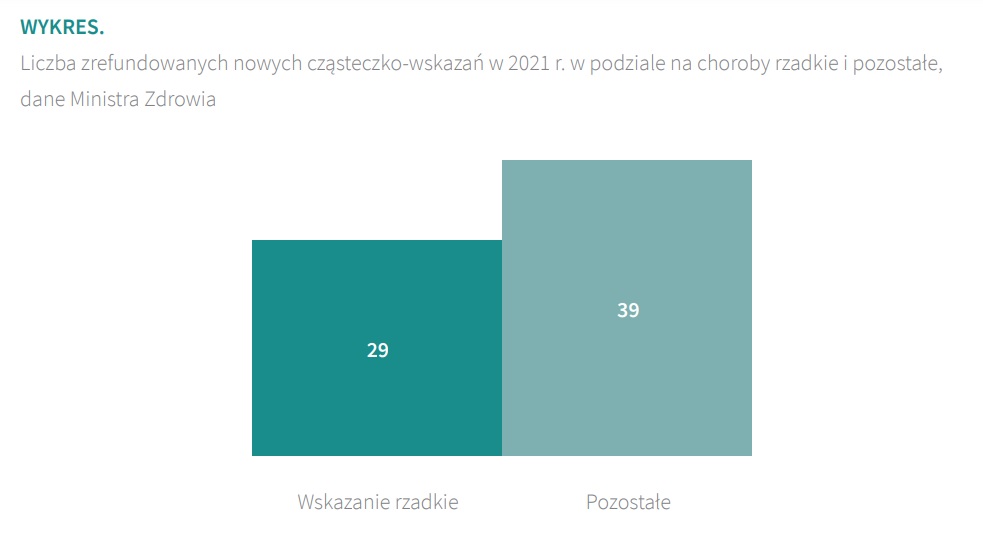
Z perspektywy systemu ochrony zdrowia choroby rzadkie dotyczą niewielkiego odsetka populacji. Leczenie jest prowadzone w wysokospecjalistycznych ośrodkach klinicznych, a leki refundowane głównie w ramach programów lekowych Narodowego Funduszu Zdrowia. W aspekcie optymalizacji modelu opieki nad chorymi na choroby rzadkie przygotowano rozwiązania i zabezpieczono finansowanie w ramach Planu dla Chorób Rzadkich na lata 2021-2023 oraz Funduszu Medycznego. Celem strategii Zdrowa Przyszłość jest zapewnienie obywatelom równego i adekwatnego do potrzeb zdrowotnych dostępu do wysokiej jakości świadczeń zdrowotnych przez przyjazny, nowoczesny i efektywny system ochrony zdrowia.1
W 2021 r. został przyjęty przez Radę Ministrów operacyjny Plan dla Chorób Rzadkich na lata 2021-2023. Plan przewiduje utworzenie krajowych ośrodków referencyjnych, określonych dla wybranej choroby rzadkiej lub grupy takich chorób, które będą pełnić kluczową rolę w integracji opieki, a także współpracujących z nimi centrów eksperckich. Ma zostać poprawiony dostęp do diagnostyki chorób rzadkich oraz leków. Ponadto mają powstać rejestry medyczne poszczególnych chorób rzadkich, platforma informacyjna oraz paszport chorego z chorobą rzadką.2
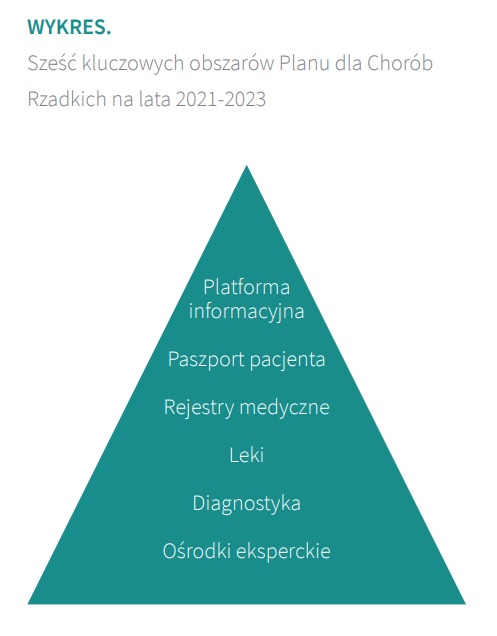
Na realizację Planu dla Chorób Rzadkich przeznaczono ok. 130 mln zł. W skład Rady ds. Chorób Rzadkich został powołany również przedstawiciel chorych na choroby rzadkie – Pan Stanisław Maćkowiak, Prezes Krajowego Forum na rzecz terapii chorób rzadkich – Orphan. Model opieki nad chorym na amyloidozę transtyretynową z kardiomiopatią (ATTR-CM) może już niedługo być w pełni spójny z założeniami uchwalonego Planu dla Chorób Rzadkich. Obecnie w Polsce działa 5 wielospecjalistycznych ośrodków eksperckich – klinik kardiologicznych, które we współpracy z pracowniami medycyny nuklearnej prowadzą kompleksową diagnostykę. Prowadzony jest również rejestr.
 Jednocześnie wielkie nadzieje chorzy na choroby rzadkie wiążą z Funduszem Medycznym, na który rocznie alokowane jest 4,2 mld zł, w tym na refundacje leków w chorobach rzadkich i onkologicznych 720 mln zł.3 W ramach Funduszu Medycznego chorzy na choroby rzadkie mogą mieć refundowane terapie w ramach wykazu leków o wysokim stopniu innowacyjności (TLI) oraz wykazu leków o wysokiej wartości klinicznej (TLK). Wykazy tych technologii opracowuje Agencja Oceny Technologii Medycznych i Taryfikacji, a zatwierdza Minister Zdrowia. Na docenienie zasługuje fakt, że w skład Rady Funduszu Medycznego zostali powołani obok klinicystów i urzędników, przedstawiciele dwóch organizacji pacjentów chorujących na choroby rzadkie – m.in. Stanisław Maćkowiak, Prezes Krajowego Forum na rzecz terapii choró rzadkich – Orphan.
Jednocześnie wielkie nadzieje chorzy na choroby rzadkie wiążą z Funduszem Medycznym, na który rocznie alokowane jest 4,2 mld zł, w tym na refundacje leków w chorobach rzadkich i onkologicznych 720 mln zł.3 W ramach Funduszu Medycznego chorzy na choroby rzadkie mogą mieć refundowane terapie w ramach wykazu leków o wysokim stopniu innowacyjności (TLI) oraz wykazu leków o wysokiej wartości klinicznej (TLK). Wykazy tych technologii opracowuje Agencja Oceny Technologii Medycznych i Taryfikacji, a zatwierdza Minister Zdrowia. Na docenienie zasługuje fakt, że w skład Rady Funduszu Medycznego zostali powołani obok klinicystów i urzędników, przedstawiciele dwóch organizacji pacjentów chorujących na choroby rzadkie – m.in. Stanisław Maćkowiak, Prezes Krajowego Forum na rzecz terapii choró rzadkich – Orphan.
Obecnie kluczowym postulatem środowiska lekarzy i pacjentów jest refundacja publiczna tafamidisu w Polsce. Tafamidis został zarejestrowany w Unii Europejskiej we wskazaniu amyloidoza serca w dniu 19 lutego 2020 r. Lek uzyskał status leku sierocego. Jest to terapia doustna. Tafamidis jest jedyną opcją terapii przyczynowej dla pacjentów chorujących na kardiomiopatię w przebiegu amyloidozy transtyretynowej (amyloidoza serca). Wyniki badań klinicznych pokazują, że włączenie nowej farmakoterapii prowadzi do redukcji liczby zgonów i przedłużenia życia chorych, zmniejszenia liczby hospitalizacji oraz wzrostu jakości życia pacjentów.
Obecnie tafamidis jest refundowany w 16 krajach UE/EFTA, tj.: Austria, Belgia, Finlandia, Francja, Irlandia, Islandia, Litwa, Luksemburg, Niemcy, Norwegia, Portugalia, Rumunia, Słowenia, Szwajcaria, Szwecja i Włochy. Dodatkowo w kolejnych krajach trwają postępowania refundacyjne, które mają na celu zwiększenie dostępności chorych do terapii.
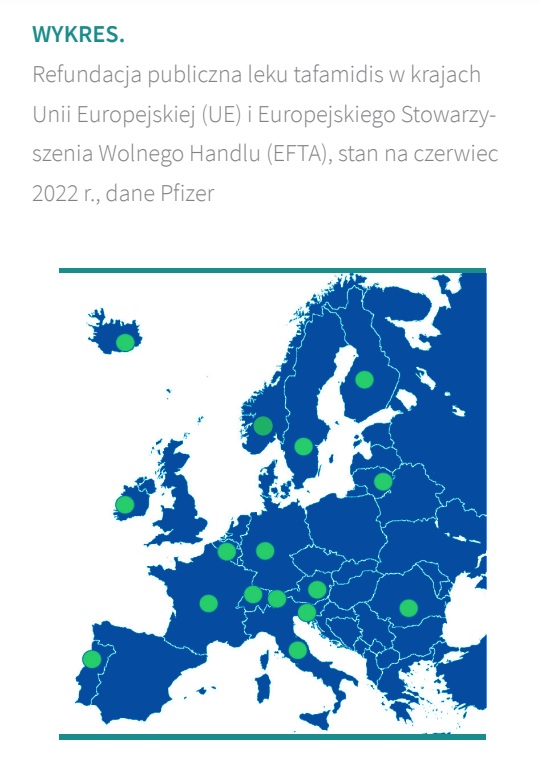
W Polsce proces refundacji leku tafamidis rozpoczął się 5 października 2021 r. W dniu 20 grudnia 2021 r. Rada Przejrzystości wydała Stanowisko nr 143/2021, a w dniu 23 grudnia 2021 r. Prezes Agencji Oceny Technologii Medycznych i Taryfikacji wydał Rekomendację nr 141/2021 w sprawie objęcia refundacją produktu leczniczego tafamidis do stosowania w ramach programu lekowego „Leczenie tafamidisem kardiomiopatii w przebiegu amyloidozy transtyretynowej u dorosłych (ICD-10 E85)”.
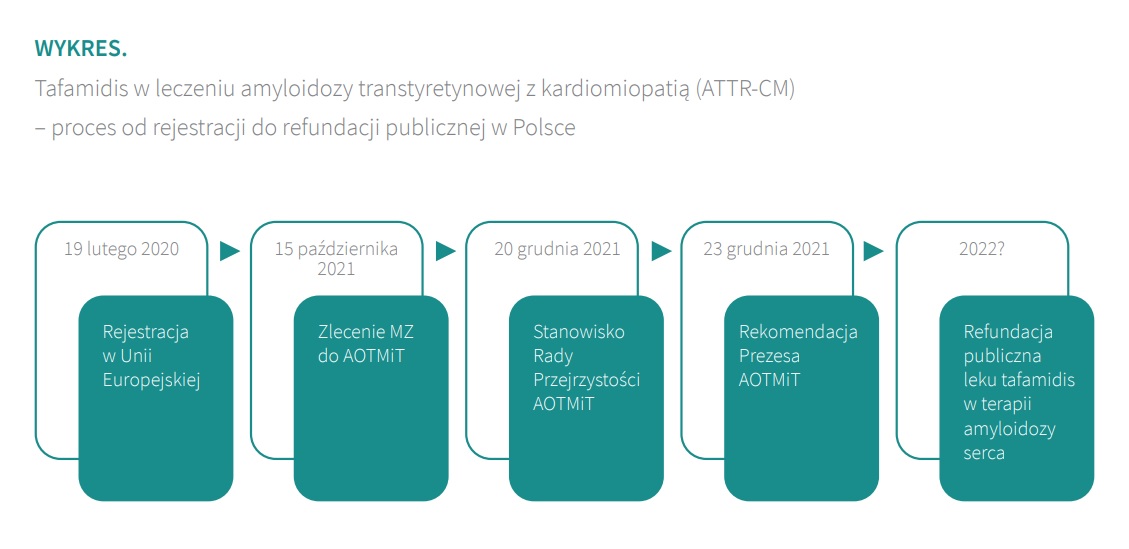 Należy pokreślić, że negatywne Stanowisko Rady Przejrzystości oraz negatywna Rekomendacja Prezesa AOTMiT uzasadnione były wyłącznie zbyt wysokim kosztem terapii tafamidisem, a nie brakiem dowodów na skuteczność tej terapii w amyloidozie serca. W swoim Stanowisku Rada Przejrzystości AOTMiT stwierdziła, że kardiomiopatia w przebiegu amyloidozy transtyretynowej (ATTR-CM) jest rzadko występującą, i jeszcze rzadziej rozpoznawaną chorobą spichrzeniową, spowodowaną gromadzeniem się w przestrzeni zewnątrzkomórkowej włókien amyloidu – transtyretyny. Skutkuje to stopniowym pogarszaniem funkcji rozkurczowej, a w bardziej zaawansowanych stadiach – także funkcji skurczowej lewej komory. Jest ona oporna na typowe leczenie niewydolności serca, co szybko prowadzi do śmierci pacjenta. Średni wiek rozpoznania to 74 lata; przeżycie od rozpoznania wynosi ok. 4 lata. Podkreśliła, że tafamidis był do tej pory stosowany głównie do leczenia neuropatii w przebiegu amyloidozy. Jego skuteczność w leczeniu ATTR-CM wykazano w wieloośrodkowym badaniu z randomizacją – ATTR-ACT. Zastosowanie tafamidisu w dawce 80 mg wiązało się z obniżeniem ryzyka złożonego punktu końcowego (śmiertelności z uwzględnieniem przyczyn oraz hospitalizacji z przyczyn sercowo naczyniowych) o 30%; był to efekt istotny pod względem statystycznym. Przez najbliższe lata ATTR-CM będzie rozpoznawana
Należy pokreślić, że negatywne Stanowisko Rady Przejrzystości oraz negatywna Rekomendacja Prezesa AOTMiT uzasadnione były wyłącznie zbyt wysokim kosztem terapii tafamidisem, a nie brakiem dowodów na skuteczność tej terapii w amyloidozie serca. W swoim Stanowisku Rada Przejrzystości AOTMiT stwierdziła, że kardiomiopatia w przebiegu amyloidozy transtyretynowej (ATTR-CM) jest rzadko występującą, i jeszcze rzadziej rozpoznawaną chorobą spichrzeniową, spowodowaną gromadzeniem się w przestrzeni zewnątrzkomórkowej włókien amyloidu – transtyretyny. Skutkuje to stopniowym pogarszaniem funkcji rozkurczowej, a w bardziej zaawansowanych stadiach – także funkcji skurczowej lewej komory. Jest ona oporna na typowe leczenie niewydolności serca, co szybko prowadzi do śmierci pacjenta. Średni wiek rozpoznania to 74 lata; przeżycie od rozpoznania wynosi ok. 4 lata. Podkreśliła, że tafamidis był do tej pory stosowany głównie do leczenia neuropatii w przebiegu amyloidozy. Jego skuteczność w leczeniu ATTR-CM wykazano w wieloośrodkowym badaniu z randomizacją – ATTR-ACT. Zastosowanie tafamidisu w dawce 80 mg wiązało się z obniżeniem ryzyka złożonego punktu końcowego (śmiertelności z uwzględnieniem przyczyn oraz hospitalizacji z przyczyn sercowo naczyniowych) o 30%; był to efekt istotny pod względem statystycznym. Przez najbliższe lata ATTR-CM będzie rozpoznawana
jedynie w ośrodkach wysokospecjalistycznych.
Rekomendacje refundacyjne w innych krajach są rozbieżne (pozytywne: kanadyjska, nowozelandzka; negatywne: brytyjska, w tym NICE, irlandzka i niderlandzka).4 W swojej Rekomendacji Prezes Agencji Oceny Technologii Medycznych i Taryfikacji stwierdził, że zastosowanie tafamidisu w dawce 80 mg wiązało się z istotnym statystycznie zmniejszeniem śmiertelności ogółem (HR = 0,690) oraz częstotliwości hospitalizacji z przyczyn sercowo-naczyniowych (RR = 0,70). Jednocześnie podkreślił, że podstawowym argumentem przeciwko finansowaniu produktu leczniczego tafamidis na zaproponowanych warunkach są wyniki analizy ekonomicznej, zgodnie z którą oszacowana wartość ICUR jest za wysoka (zbyt wysoka cena leku).5
W swojej analizie weryfikacyjnej Agencja Oceny Technologii Medycznych i Taryfikacji podkreśliła, że w wyniku wyszukiwania odnaleziono 3 rekomendacje pozytywne (HAS 2020, PHARMAC 2019 i CADTH 2020) i 4 rekomendacje negatywne (SMC 2021, Zorginstituut 2021, NICE 2021 i NCPE 2020) dotyczące refundowania leku tafamidis w leczeniu kardiomiopatii w przebiegu ATTR. Kanadyjskie CADTH wydał rekomendację pozytywną pod warunkiem redukcji ceny leku, natomiast PHARMAC rekomenduje finansowanie terapii tafamidisem ze średnim priorytetem. W rekomendacjach pozytywnych zwraca się głównie uwagę na brak finansowania alternatywnych środków farmaceutycznych modyfikujących postęp choroby, istotne korzyści kliniczne oraz korzystny stosunek skuteczności leku do działań niepożądanych.
W rekomendacjach negatywnych zwraca się głównie uwagę na brak efektywności kosztowej oraz niespójne wyniki dotyczące skuteczności tafamidisu w różnych typach i stadiach ATTR-CM.6 Należy podkreślić, że wnioskowana terapia tafamidisem dotyczy tylko estymowanych ok. 109 pacjentów leczonych w I roku od wejścia w życie programu lekowego, z których 42, to nowi pacjenci oraz 141 potencjalnie leczonych pacjentów w II roku refundacji publicznej tafamidisu (z których 51, to nowi pacjenci).

Piśmiennictwo:
- Zdrowa Przyszłość. Ramy strategiczne rozwoju systemu ochrony zdrowia na lata 2021-2027, z perspektywą do 2030. https://www.gov.pl/web/zdrowie/zdrowa-przyszlosc-ramy-strategiczne-rozwoju-systemu-ochrony-zdrowia-na-lata-2021-2027-z-perspektywa-do-2030
- Uchwała nr 110 Rady Ministrów z dnia 24 sierpnia 2021 r. w sprawie przyjęcia dokumentu Plan dla Chorób Rzadkich. https://isap.sejm.gov.pl/isap.nsf/DocDetails.xsp?id=WMP20210000883
- Ustawa z dnia 7 października 2020 r. o Funduszu Medycznym. https://isap.sejm.gov.pl/isap.nsf/DocDetails.xsp?id=WDU20200001875
- Stanowisko Rady Przejrzystości nr 143/2021 z dnia 20 grudnia 2021 roku w sprawie oceny leku Vyndaqel (tafamidisum) w ramach programu lekowego „Leczenie tafamidisem kardiomiopatii w przebiegu amyloidozy transtyretynowej u dorosłych (ICD-10 E85)”. AOTMiT, 2021. https://bipold.aotm.gov.pl/assets/files/zlecenia_mz/2021/146/SRP/U_56_332_20122021_s_143_Vyndaqel_tafamidisum_w_ref_prop_REOPTR.pdf
- Rekomendacja nr 141/2021 z dnia 23 grudnia 2021 r. Prezesa Agencji Oceny Technologii Medycznych i Taryfikacji w sprawie objęcia refundacją produktu leczniczego tafamidis, kapsułki miękkie, 61 mg, 30 kaps. (1 × 30), kod GTIN: 05415062359426 do stosowania w ramach programu lekowego „Leczenie tafamidisem kardiomiopatii w przebiegu amyloidozy transtyretynowej u dorosłych (ICD-10 E85)”. AOTMiT, 2021 https://bipold.aotm.gov.pl/assets/files/zlecenia_mz/2021/146/REK/2021_12_23_BP_Rekomendacja_141-2021_Vyndaqel_BIP_REOPTR.pdf
- Wniosek o objęcie refundacją i ustalenie urzędowej ceny zbytu produktu leczniczego tafamidis w ramach programu lekowego leczenia kardiomiopatii wprzebiegu amyloidozy transtyretynowej u dorosłych (ICD-10 E85). Analiza weryfikacyjna. Nr OT.4231.49.2021. AOTMiT, 2021. https://bipold.aotm.gov.pl/assets/files/zlecenia_mz/2021/146/AWA/146_OT.4231.49.2021_Vyndaqel_BIP_REOPTR.pdf
