
Do najczęstszych postaci amyloidozy należą amyloidoza łańcuchów lekkich immunoglobulin (amyloidoza AL) oraz amyloidoza transtyretynowa (ATTR) zarówno dziedziczna (ATTRv), jak i typu dzikiego (ATTRwt). Choroby te wiążą się nie tylko z ciężkimi objawami narządowymi, ale również z licznymi problemami żywieniowymi, które znacząco wpływają na przebieg kliniczny, rokowanie i jakość życia pacjentów.

Wiedza, doświadczenie i najnowsze osiągnięcia w diagnostyce oraz terapii amyloidozy – choroby, która wymaga skoordynowanego podejścia wielu specjalności medycznych. Prezentacje specjalistów z wydarzenia są już dostępne w formie relacji cyfrowych.

Amyloidoza serca (CA, cardiac amyloidosis) to trudna do rozpoznania i dlatego często zbyt późno wykrywana choroba o wysokiej śmiertelności, która znacząco wpływa na funkcjonowanie fizyczne i psychiczne pacjentów. W ostatnich latach coraz większą uwagę poświęca się aspektom psychologicznym tej choroby, zwłaszcza zaburzeniom lękowym i depresyjnym. Niniejsza praca stanowi pierwszą systematyczną analizę literatury dotyczącą związku między CA a występowaniem zaburzeń lękowych i depresji.
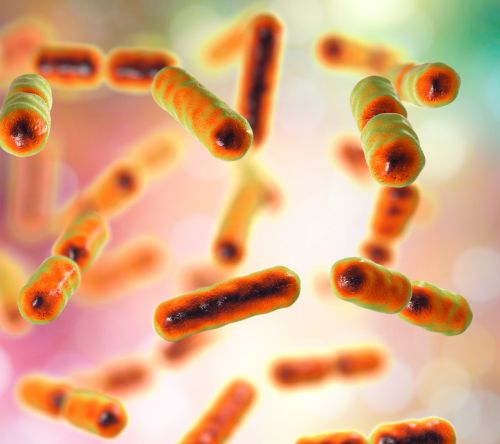
Amyloidoza transtyretynowa (amyloidoza ATTR) jest chorobą ogólnoustrojową, w której dochodzi do odkładania amyloidu zbudowanego z transtyretyny w różnych tkankach, w tym w sercu i przewodzie pokarmowym. Zaburzenia perfuzji, obrzęk błony śluzowej jelit oraz zaburzenia układu autonomicznego mogą prowadzić do zmian w składzie mikrobiomu jelitowego. Celem omawianego badania była analiza różnic w składzie mikrobiomu jelitowego u pacjentów z amyloidozą ATTR z zajęciem serca, bez zajęcia serca oraz w grupie kontrolnej, a także ocena korelacji między zmianami mikrobiomu a parametrami klinicznymi, biochemicznymi i echokardiograficznymi.

W dobie dynamicznego rozwoju narzędzi obrazowania medycznego, jednym z najbardziej przełomowych kroków w obszarze diagnostyki kardiologicznej jest zastosowanie scyntygrafii w rozpoznawaniu amyloidozy serca. To nowy standard, który wyznacza kierunek skutecznej diagnostyki rzadkiej, a zarazem coraz częściej występującej choroby w populacji pacjentów w podeszłym wieku.

Amyloidoza łańcuchów lekkich (amyloidoza AL) jest rzadką chorobą układową, w której zajęcie nerek występuje u około 70% pacjentów i odpowiada za blisko 1% przypadków schyłkowej niewydolności nerek wymagającej leczenia nerkozastępczego (RRT). Rokowanie w amyloidozie AL zależy zarówno od stopnia zajęcia serca, jak i od dynamiki progresji uszkodzenia nerek.

Amyloidoza jest chorobą wynikającą z odkładania się w tkankach złogów białek o nieprawidłowej konformacji, które tworzą włókna amyloidowe. Może obejmować różne narządy, w tym serce, nerwy obwodowe, przewód pokarmowy i nerki. W przypadku amyloidozy z zajęciem serca (CA) aż 95% przypadków stanowią dwie główne postaci: amyloidoza transtyretynowa (ATTR) – dzieląca się na dziedziczną (ATTRv) i dziką (ATTRwt) oraz amyloidoza łańcuchów lekkich (amyloidoza AL). Choroby te występują głównie u osób starszych, zwłaszcza po 70. roku życia i są coraz częściej rozpoznawane dzięki wzrostowi świadomości klinicystów i powszechnym wykorzystaniu nieinwazyjnych metod diagnostycznych.

Wiedza, doświadczenie i najnowsze osiągnięcia w diagnostyce oraz terapii amyloidozy – choroby, która wymaga skoordynowanego podejścia wielu specjalności medycznych. Serdecznie zapraszamy do udziału w IX Interdyscyplinarnej Konferencji Amyloidoza, która odbędzie się w dniach 3-4 października 2025 r. w formule on-line.

Zapraszamy do obejrzenia nagrania prof. Krzysztofa Jamroziaka, w którym zostały szczegółowo omówione najważniejsze i najnowsze doniesienia dotyczące rzadkich dyskrazji plazmocytowych, ze szczególnym uwzględnieniem amyloidozy AL. W swojej prezentacji ekspert dzieli się wybranymi, najbardziej wartościowymi wnioskami z międzynarodowych konferencji i badaniami, które bezpośrednio wpływają na codzienną praktykę hematologiczną w Polsce.

W ostatnich latach leczenie amyloidozy ATTR i kardiomiopatii w przebiegu tej choroby uległo zasadniczej zmianie. Istnieją na razie trzy klasy mechanizmów terapeutycznych: stabilizatory tetrameru TTR, leki wyciszające ekspresję TTR oraz strategie deplecyjne ukierunkowane na złogi. Leczenie choroby wchodzi w etap wielości skutecznych opcji, ale konieczna jest indywidualizacja wyboru terapii z uwzględnieniem fenotypu pacjenta, dostępności i kosztów oraz ustrukturyzowane monitorowanie leczenia. Priorytetem są badania nad terapią skojarzoną, wypracowanie ram porównawczych i punktów końcowych dla nowych badań klinicznych oraz strategie zapewniające równość dostępu do leczenia.
Amyloidoza łańcuchów lekkich (amyloidoza AL) jest rzadką chorobą układu krwiotwórczego, wywoływaną przez klonalne komórki plazmatyczne produkujące patogenne łańcuchy lekkie immunoglobulin, które ulegają odkładaniu w narządach wewnętrznych, prowadząc do ich uszkodzenia.
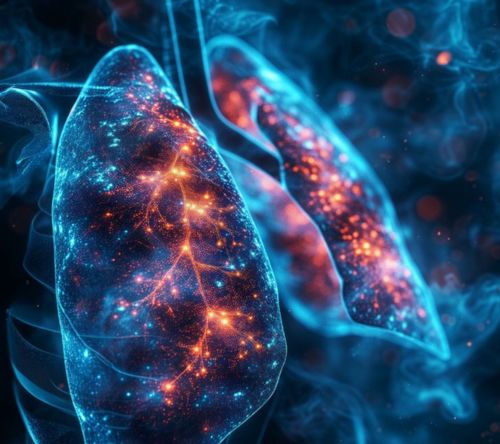
Układowa amyloidoza łańcuchów lekkich (amyloidoza AL) to rzadka choroba klonalna/dyskrazja plazmocytowa spowodowana odkładaniem się źle sfałdowanych monoklonalnych łańcuchów lekkich w narządach wewnętrznych. Chociaż amyloid najczęściej odkłada się w sercu i nerkach, może również gromadzić się w miąższu płuc, prowadząc do objawów ze strony układu oddechowego.
Amyloidoza serca (cardiac amyloidosis, CA), w tym postać transtyretynowa (ATTR-CA), stanowi ważną, choć często nierozpoznaną przyczynę niewydolności serca, szczególnie u pacjentów w podeszłym wieku.
Amyloidoza łańcuchów lekkich (amyloidoza AL) to rzadka, lecz potencjalnie śmiertelna choroba związana z odkładaniem nieprawidłowych złogów amyloidu w tkankach. Są one produkowane przez klonalne plazmocyty wytwarzające łańcuchy lekkie immunoglobulin. Objawy kliniczne są zróżnicowane i zależą od zajętych narządów, przy czym zajęcie serca pozostaje najistotniejszym czynnikiem rokowniczym.
Gammopatia monoklonalna o nieustalonym znaczeniu (MGUS) jest często wykrywana przypadkowo i wiąże się ze zwiększonym ryzykiem rozwoju szpiczaka plazmocytowego (MM). Rzadziej może dochodzić również do progresji do innych chorób związanych z komórkami plazmatycznymi – w tym amyloidozy łańcuchów lekkich (amyloidozy AL).
Amyloidoza transtyretynowa z zajęciem serca (ATTR-CA) należy do kardiomiopatii restrykcyjnych spowodowanych odkładaniem się amyloidu zbudowanego z białka transtyretyny w przestrzeniach międzykomórkowych kardiomiocytów.
- « Poprzednia
- 1
- 2
- 3
- 4
- 5
- …
- 25
- 26
- 27
- Następna »